目前,页岩气及煤层气固—气吸附体系的吸附热力学分析主要采用基于Clausius-Clapeyron方程的等量线标绘法计算等量吸附热,研究结果一致表明等量吸附热与吸附量间满足良好的线性单调性的变化规律
[4-15]。不同固—气吸附体系的等量吸附热,除在相同吸附量下,吸附热值的大小存在差异外,等量吸附热与吸附量间的线性特征亦存在差异,具体而言煤岩
[4-7]及四川盆地南部龙马溪组页岩
[8]吸附CH
4的等量吸附热与吸附量间满足线性正相关,而牛蹄塘组页岩及柴达木盆地石炭系页岩则为线性负相关
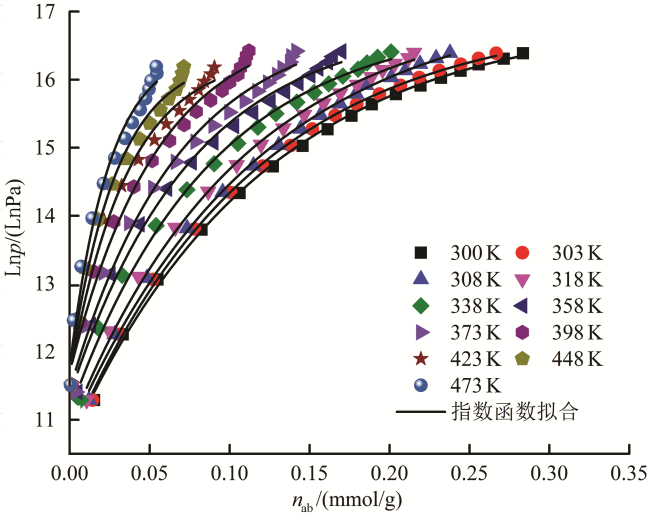
[9-11]。由于等量线标绘法是以不同温度下吸附体系的等温吸附量作为数据基础,利用压力的自然对数Ln
p与吸附量
n曲线的拟合函数,计算并绘制不同吸附量
n下的Ln
p与温度倒数1/
T的曲线,进而利用Ln
p—1/
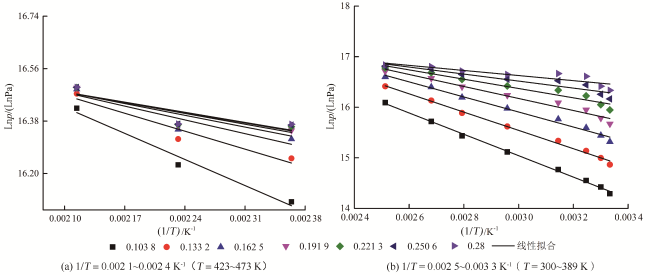
T曲线的线性拟合斜率计算等量吸附热,因此计算结果只能反映相应温度范围及对应吸附量区间内的热力学特征。现有研究
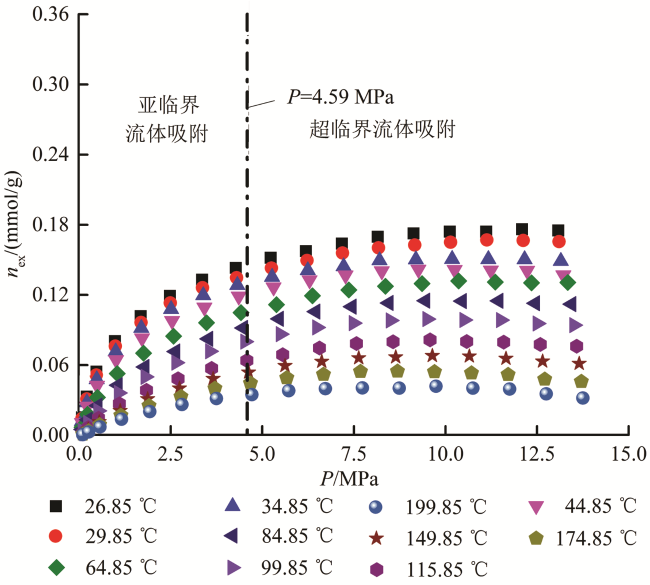
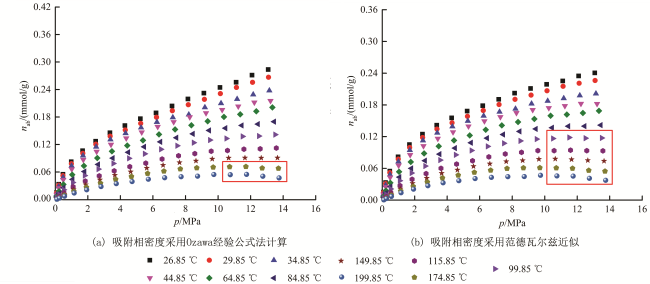
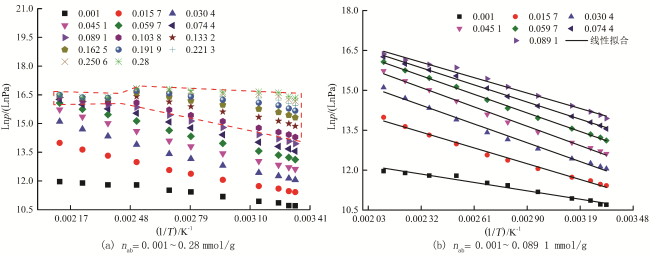
[4-15]在等量吸附热计算过程均采用了过剩吸附量作为等量吸附热计算的基础数据,而过剩吸附量并不能真实反映吸附体系的实际吸附量。同时计算过程中仅针对Ln
p—
n曲线中吸附量
n的某一局部区间进行了Ln
p—1/
T曲线的计算,所得出的结论也仅能反映该吸附量局部区间内的热力学特征,无法全面反映整个吸附过程中的热力学变化。与此同时,现有研究中等温吸附曲线的测定温度主要集中在15~70 ℃之间
[4-15],随着平衡温度的升高,吸附质分子的分子动能增加,页岩及煤岩对气体分子的吸附能力下降,因此在更高温度范围内的等量吸附热特性,必然与现有的认识存在一定的差异。


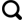
 甘公网安备 62010202000678号
甘公网安备 62010202000678号