0 引言
1 研究区地质概况
2 样品采集与实验方法
2.1 样品采集
2.2 实验分析方法
2.2.1 TOC及有机碳同位素
2.2.2 总碳(TC)及总氮(TN)
2.2.3 有机质抽提、分离及色谱—质谱仪分析
3 实验结果及有机地球化学特征
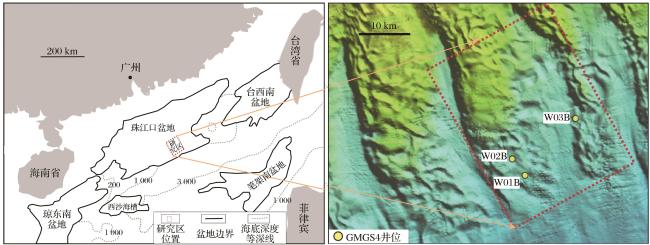
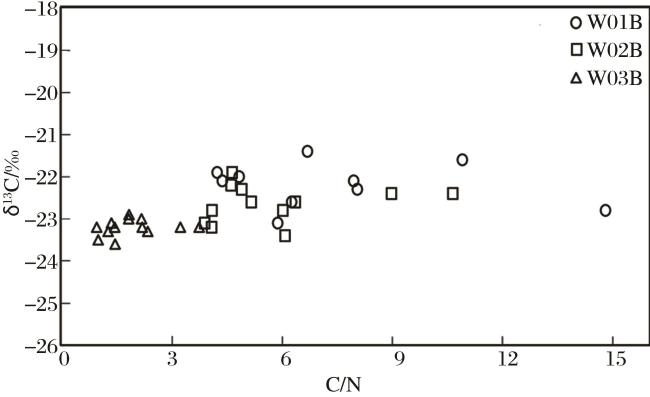
3.1 沉积物中碳氮含量特征
表1 3个站位TOC、TN、TC、C/N和δ13C数据Table 1 Data of TOC, TN, TC、C/N and δ13C for three sites |
| 站位 | 采样深度 /mbsf | TOC/% | TN/% | TC/% | C/N | δ13C /‰ |
|---|---|---|---|---|---|---|
| W01B | 54.90 | 1.17 | 0.147 1 | 2.403 2 | 7.95 | -22.1 |
| 111.90 | 0.27 | 0.061 8 | 4.805 4 | 4.37 | -22.1 | |
| 119.52 | 0.26 | 0.044 2 | 5.019 8 | 5.88 | -23.1 | |
| 127.90 | 0.36 | 0.053 8 | 4.758 9 | 6.69 | -21.4 | |
| 134.15 | 0.30 | 0.047 9 | 5.298 7 | 6.26 | -22.6 | |
| 145.48 | 0.20 | 0.041 4 | 6.861 | 4.83 | -22.0 | |
| 165.77 | 0.44 | 0.029 7 | 3.913 2 | 14.81 | -22.8 | |
| 166.88 | 0.36 | 0.033 | 3.392 1 | 10.91 | -21.6 | |
| 178.26 | 0.31 | 0.038 5 | 3.214 8 | 8.05 | -22.3 | |
| 192.77 | 0.21 | 0.049 7 | 2.732 4 | 4.23 | -21.9 | |
| W02B | 44.90 | 0.77 | 0.157 2 | 3.079 4 | 4.90 | -22.3 |
| 83.90 | 0.56 | 0.108 5 | 3.691 8 | 5.16 | -22.6 | |
| 99.90 | 0.40 | 0.065 8 | 4.812 1 | 6.08 | -23.4 | |
| 106.86 | 0.49 | 0.077 1 | 3.13 | 6.36 | -22.6 | |
| 116.74 | 0.37 | 0.061 5 | 4.270 7 | 6.02 | -22.8 | |
| 128.69 | 0.36 | 0.033 8 | 5.126 1 | 10.65 | -22.4 | |
| 137.41 | 0.30 | 0.033 4 | 4.387 7 | 8.98 | -22.4 | |
| 153.85 | 0.23 | 0.049 9 | 3.070 7 | 4.61 | -22.2 | |
| 166.01 | 0.18 | 0.038 8 | 2.947 8 | 4.64 | -21.9 | |
| 173.64 | 0.22 | 0.053 8 | 2.575 3 | 4.09 | -22.8 | |
| 176.81 | 0.18 | 0.046 3 | 2.510 2 | 3.89 | -23.1 | |
| 189.90 | 0.27 | 0.066 2 | 2.693 | 4.08 | -23.2 | |
| W03B | 47.90 | 0.04 | 0.041 9 | 1.721 2 | 0.95 | -23.2 |
| 94.43 | 0.07 | 0.038 3 | 1.617 3 | 1.83 | -22.9 | |
| 131.90 | 0.07 | 0.048 6 | 1.598 1 | 1.44 | -23.2 | |
| 149.43 | 0.09 | 0.062 | 1.833 6 | 1.45 | -23.6 | |
| 154.15 | 0.08 | 0.063 4 | 1.657 1 | 1.26 | -23.3 | |
| 170.85 | 0.12 | 0.066 | 1.832 2 | 1.82 | -23 | |
| 176.36 | 0.08 | 0.059 1 | 1.702 2 | 1.35 | -23.1 | |
| 190.65 | 0.15 | 0.064 1 | 1.697 2 | 2.34 | -23.3 | |
| 199.47 | 0.15 | 0.069 2 | 1.502 6 | 2.17 | -23 | |
| 204.28 | 0.15 | 0.068 6 | 1.773 6 | 2.19 | -23.2 | |
| 210.08 | 0.22 | 0.068 2 | 1.766 9 | 3.23 | -23.2 | |
| 213.90 | 0.26 | 0.069 5 | 1.677 7 | 3.74 | -23.2 | |
| 218.00 | 0.20 | 0.203 | 2.089 1 | 0.99 | -23.5 |
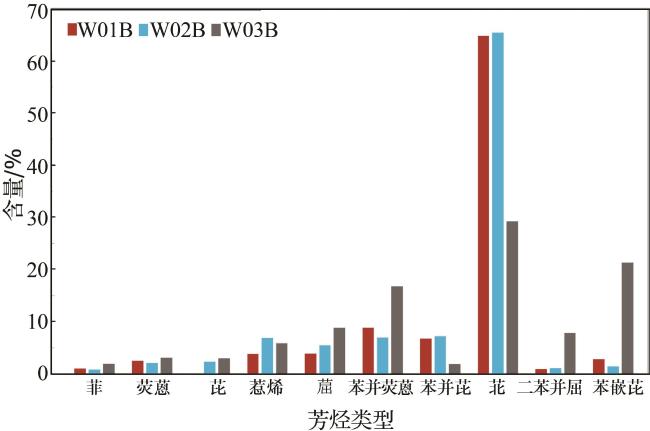
3.2 可溶有机质特征
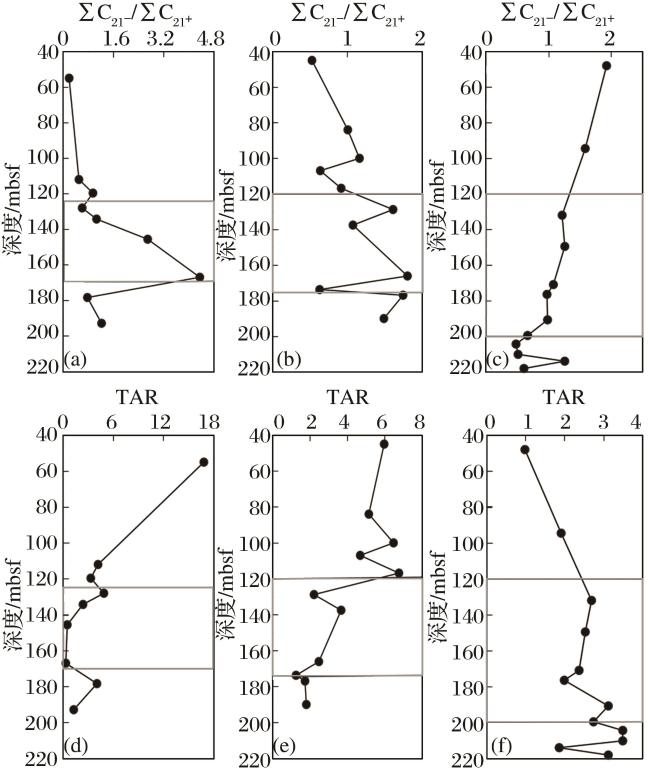
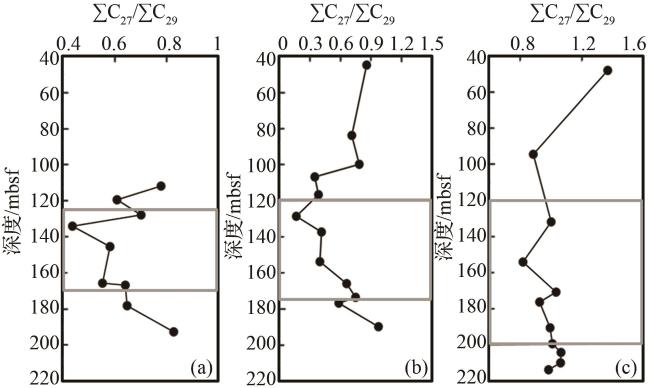
3.3 物源组成的差异解释
3.4 物源特征异常及生物降解
4 微生物降解作用及指标选择
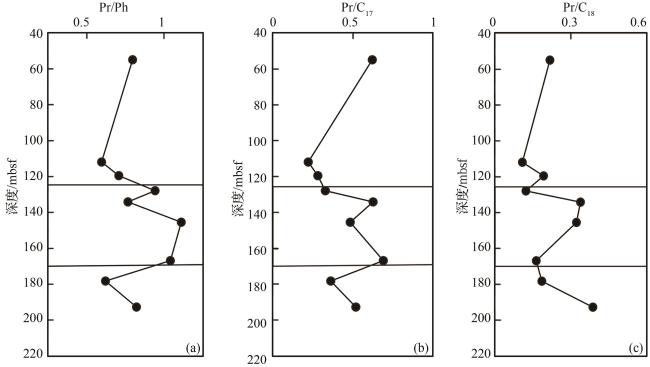
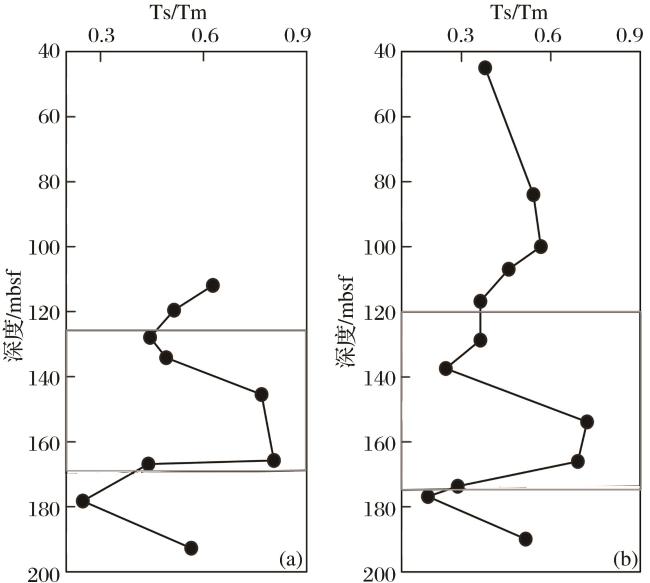
4.1 生物降解指标
表2 3个站位深海沉积物生物指标特征 (平均)Table 2 Biological characteristics of deep-sea sediments at three sites (average) |
| 生物指标类型 | W01B-N | W01B-NGH | W02B-N | W02B-NGH | W03B-N | W03B-NGH |
|---|---|---|---|---|---|---|
| 氯仿沥青“A”/% | 0.009 3 | 0.009 9 | 0.007 3 | 0.005 4 | 0.003 4 | 0.007 7 |
| N/% | 22.22 | 25.86 | 21.99 | 21.29 | 31.83 | 20.25 |
| A/% | 6.42 | 4.36 | 6.57 | 8.72 | 4.50 | 5.32 |
| (F+沥青)/% | 69.55 | 69.78 | 71.44 | 69.99 | 63.67 | 74.43 |
| N/A | 3.54 | 5.63 | 3.45 | 3.65 | 7.49 | 4.29 |
| (N+A)/TOC | 96.65 | 114.54 | 83.36 | 132.26 | 332.01 | 243.70 |
| TOC/% | 0.43 | 0.33 | 0.40 | 0.24 | 0.16 | 0.11 |
| 0.70 | 2.18 | 0.86 | 0.79 | 1.18 | 0.87 | |
| OEP1 | 0.29 | 0.43 | 0.23 | 0.18 | 0.39 | 0.35 |
| OEP2 | 4.45 | 3.67 | 4.78 | 3.48 | 3.59 | 3.38 |
| nC15—nC19 | 1.26 | 2.35 | 1.58 | 4.25 | 5.01 | 10.27 |
| nC20—nC24 | 2.14 | 2.91 | 1.88 | 2.96 | 7.00 | 8.97 |
| nC25—nC30 | 1.74 | 3.17 | 1.61 | 4.07 | 4.11 | 6.44 |
| iC18—iC20 | 7.85 | 11.31 | 9.82 | 19.02 | 18.02 | 41.71 |
| 角鲨烷/% | 4.10 | 4.55 | 4.52 | 4.57 | 5.53 | 8.30 |
|
表3 3个站位微生物降解指标Table 3 Biodegradation indicators for three sites |
| 样名 | 深度/mbsf | 氯仿沥青“A”/% | N /% | A /% | (F+沥青) /% | N/A | (N+A) /TOC | TOC | / | OEP1 | OEP2 | nC15—nC19 | nC20—nC24 | nC25—nC30 | iC18—iC20 | 角鲨烷 /% |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1B-2H | 54.90 | 0.027 0 | 13.45 | 5.65 | 80.89 | 2.38 | 16.33 | 1.17 | 0.1863 | 0.314 | 8.333 | |||||
| 1B-4H | 111.90 | 0.004 6 | 17.69 | 7.07 | 64.35 | 2.50 | 91.71 | 0.27 | 0.499 | 0.192 | 4.338 | 0.83 | 0.93 | 0.75 | 6.78 | 5.85 |
| 1B-5H | 119.52 | 0.008 3 | 24.25 | 7.00 | 68.75 | 3.46 | 120.19 | 0.26 | 0.945 | 0.215 | 4.219 | 0.77 | 1.14 | 1.39 | 3.91 | 2.73 |
| 1B-6H | 127.90 | 0.006 3 | 24.38 | 7.06 | 68.56 | 3.45 | 87.33 | 0.36 | 0.603 | 0.257 | 3.623 | 0.83 | 1.13 | 0.80 | 5.99 | 5.16 |
| 1B-7X | 134.15 | 0.006 6 | 26.57 | 6.79 | 66.64 | 3.91 | 111.21 | 0.30 | 1.06 | 0.288 | 3.894 | 0.47 | 0.85 | 0.86 | 2.32 | 5.16 |
| 1B-10X | 145.48 | 0.007 9 | 40.11 | 6.87 | 53.01 | 5.84 | 234.93 | 0.20 | 2.689 | 0.506 | 2.13 | 0.24 | 1.15 | 1.59 | 1.17 | 1.58 |
| 1B-16X | 165.77 | 0.015 7 | 0.19 | 0.85 | 98.96 | 0.22 | 2.36 | 0.44 | 0.638 | 0.449 | 5.478 | 8.36 | 7.81 | 6.96 | 40.05 | 10.06 |
| 1B-17X | 166.88 | 0.009 2 | 36.56 | 2.92 | 60.52 | 12.53 | 109.67 | 0.36 | 4.349 | 0.469 | 3.196 | 0.32 | 1.83 | 3.25 | 1.70 | 1.38 |
| 1B-20X | 178.26 | 0.004 6 | 23.60 | 6.56 | 69.85 | 3.60 | 97.27 | 0.31 | 0.768 | 0.25 | 3.596 | 2.37 | 3.76 | 2.67 | 11.63 | 3.57 |
| 1B-23X | 192.77 | 0.005 2 | 29.94 | 5.15 | 64.92 | 5.82 | 167.07 | 0.21 | 1.22 | 0.537 | 2.574 | 1.49 | 3.75 | 3.07 | 10.93 | 3.20 |
| 2B-1H | 44.90 | 0.009 9 | 12.99 | 3.14 | 83.87 | 4.13 | 20.95 | 0.77 | 0.42 | 0.359 | 4.258 | 6.83 | 4.17 | 2.52 | 30.27 | 7.84 |
| 2B-3H | 83.90 | 0.009 3 | 23.28 | 4.64 | 72.08 | 5.02 | 49.86 | 0.56 | 0.803 | 0.192 | 8.395 | 1.13 | 1.74 | 1.48 | 7.63 | 2.56 |
| 2B-4H | 99.90 | 0.006 2 | 24.53 | 7.25 | 68.23 | 3.38 | 79.43 | 0.40 | 0.928 | 0.108 | 5.502 | 0.65 | 1.27 | 1.11 | 6.01 | 3.70 |
| 2B-6H | 106.86 | 0.005 8 | 29.68 | 8.71 | 61.61 | 3.41 | 78.34 | 0.49 | 0.509 | 0.377 | 4.152 | 1.08 | 1.13 | 0.88 | 3.53 | 4.93 |
| 2B-7H | 116.74 | 0.004 3 | 28.33 | 6.87 | 64.80 | 4.12 | 95.14 | 0.37 | 0.732 | 0.16 | 5.192 | 0.72 | 1.06 | 0.82 | 7.34 | 4.03 |
| 2B-9H | 128.69 | 0.010 3 | 23.51 | 9.65 | 66.83 | 2.44 | 92.13 | 0.36 | 1.287 | 0.204 | 3.419 | 1.15 | 2.04 | 2.25 | 10.56 | 5.03 |
| 2B-11X | 137.41 | 0.004 7 | 33.25 | 5.06 | 61.69 | 6.57 | 127.71 | 0.30 | 0.858 | 0.245 | 4.14 | 2.18 | 3.37 | 2.41 | 14.43 | 4.68 |
| 2B-16X | 153.85 | 0.001 9 | 0.89 | 14.24 | 84.87 | 0.06 | 65.80 | 0.23 | 0.066 | 0.104 | 2.422 | 9.37 | 2.62 | 7.11 | 33.66 | 5.49 |
| 2B-19X | 166.01 | 0.006 6 | 29.73 | 6.86 | 63.41 | 4.33 | 203.28 | 0.18 | 1.441 | 0.201 | 3.868 | 1.19 | 2.90 | 2.68 | 8.98 | 3.50 |
| 2B-21X | 173.64 | 0.005 2 | 27.16 | 7.79 | 65.05 | 3.49 | 158.85 | 0.22 | 0.502 | 0.123 | 3.826 | 0.67 | 0.82 | 0.50 | 5.95 | 3.42 |
| 2B-22X | 176.81 | 0.008 5 | 10.99 | 4.79 | 84.22 | 2.29 | 87.65 | 0.18 | 1.394 | 0.26 | 5.115 | 0.86 | 1.88 | 2.43 | 9.05 | 3.24 |
| 2B-25X | 189.90 | 0.006 3 | 17.45 | 6.28 | 76.27 | 2.78 | 87.90 | 0.27 | 1.189 | 0.317 | 3.166 | 1.11 | 2.81 | 2.53 | 8.03 | 5.92 |
| 3B-1H | 47.90 | 0.002 6 | 27.67 | 4.33 | 67.99 | 6.39 | 800.14 | 0.04 | 1.924 | 0.346 | 3.399 | 0.86 | 2.84 | 2.85 | 8.91 | 3.71 |
| 3B-3X | 94.43 | 0.002 7 | 14.76 | 5.09 | 80.15 | 2.90 | 283.64 | 0.07 | 1.583 | 0.236 | 3.118 | 1.00 | 2.64 | 2.81 | 9.43 | 6.70 |
| 3B-6X | 131.90 | 0.022 1 | 19.66 | 5.26 | 75.07 | 3.74 | 356.10 | 0.07 | 1.214 | 0.235 | 4.061 | 2.42 | 5.72 | 5.42 | 18.70 | 6.66 |
| 3B-11X | 149.43 | 0.011 1 | 23.83 | 5.62 | 70.54 | 4.24 | 327.30 | 0.09 | 1.256 | 0.222 | 3.531 | 2.60 | 6.01 | 5.49 | 20.72 | 6.42 |
| 3B-12X | 154.15 | 0.006 2 | 0.97 | 7.99 | 91.03 | 0.12 | 112.09 | 0.08 | 0.288 | 0.387 | 1.85 | 53.34 | 24.47 | 18.95 | 207.90 | 10.58 |
| 3B-17X | 170.85 | 0.005 4 | 32.91 | 4.75 | 62.34 | 6.93 | 313.83 | 0.12 | 1.074 | 0.302 | 3.532 | 2.22 | 5.14 | 3.51 | 14.89 | 5.13 |
| 3B-18X | 176.36 | 0.003 7 | 20.85 | 4.86 | 74.29 | 4.29 | 321.36 | 0.08 | 0.972 | 0.371 | 3.456 | 2.96 | 5.97 | 3.84 | 16.42 | 6.00 |
| 3B-22X | 190.65 | 0.008 0 | 17.70 | 5.83 | 76.47 | 3.04 | 156.83 | 0.15 | 0.981 | 0.248 | 3.871 | 2.26 | 4.70 | 3.75 | 12.25 | 10.44 |
| 3B-24X | 199.47 | 0.003 4 | 14.48 | 4.62 | 80.90 | 3.14 | 127.30 | 0.15 | 0.662 | 0.473 | 3.426 | 6.02 | 7.88 | 4.57 | 18.42 | 13.19 |
| 3B-25X | 204.28 | 0.001 3 | 31.62 | 3.60 | 64.78 | 8.79 | 234.82 | 0.15 | 0.477 | 0.556 | 3.302 | 10.36 | 11.83 | 6.01 | 24.41 | 8.01 |
| 3B-26X | 210.08 | 0.004 0 | 43.67 | 3.32 | 53.01 | 13.14 | 213.61 | 0.22 | 0.51 | 0.477 | 3.264 | 14.85 | 14.66 | 7.47 | 32.04 | 6.90 |
| 3B-27X | 213.90 | 0.003 0 | 39.43 | 4.96 | 55.61 | 7.96 | 170.72 | 0.26 | 1.255 | 0.403 | 5.164 | 0.69 | 1.51 | 1.17 | 2.09 | 6.05 |
| 3B-28X | 218.00 | 0.004 8 | 33.61 | 4.78 | 61.61 | 7.04 | 191.95 | 0.2 | 0.604 | 0.506 | 2.997 | 7.64 | 13.35 | 6.27 | 37.63 | 4.28 |
|
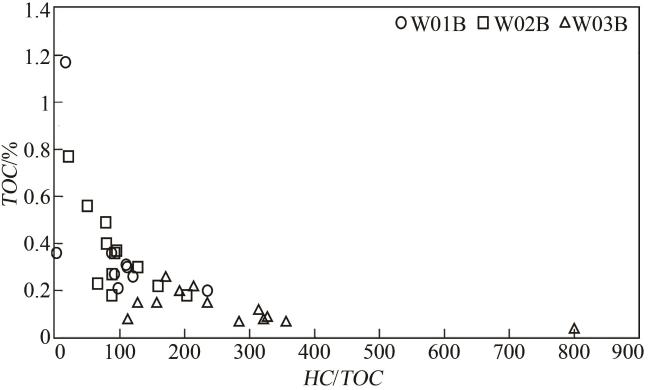
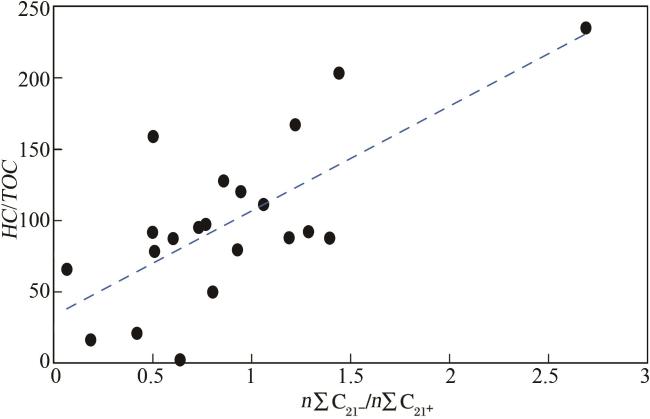
4.2 烃转换率与有机质含量降解特征
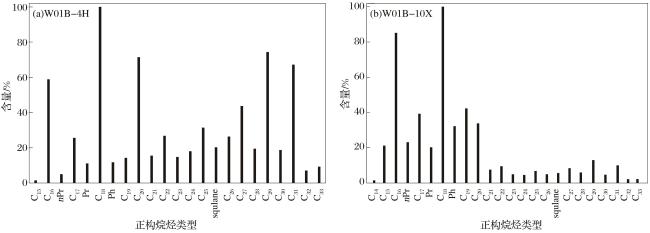
4.3 正构烷烃微生物降解特征
图8 W01B-4H(非水合物层)和W01B-10X(水合物层)正构烷烃气相色谱柱状图(相对值)Fig.8 Gas chromatographic column diagrams of n-alkanes for W01B-4H(non-hydrate layer) and W01B-10X(hydrate layer) (relative values) |


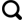
 甘公网安备 62010202000678号
甘公网安备 62010202000678号