0 引言
1 区域地质背景
2 样品和实验
3 结果
表1 沁水盆地煤层气井排采水样品的相关信息Table 1 Information of CBM co-produced water from Qinshui Basin |
| 编号 | 区块 | 样品编号 | 采样时间(年.月) | 井深/m | 开采煤层 | 累计产气量/m3 | 日产气量/(m3/d) | 开采时间(年.月) |
|---|---|---|---|---|---|---|---|---|
| 1 | 古交 | GJ08 | 2023.02 | 328 | #8 | - | 264 | 2013.02 |
| 2 | 古交 | GJ06 | 2023.02 | 316 | #2, #8 | - | 900 | 2013.01 |
| 3 | 古交 | GJ07 | 2023.02 | 382 | #8 | - | 240 | 2013.02 |
| 4 | 古交 | GJ05 | 2023.02 | 377 | #8 | - | 312 | 2013.03 |
| 5 | 古交 | GJ04 | 2023.02 | 438 | #8 | - | 0 | 2013.02 |
| 6 | 古交 | GJ03 | 2023.02 | 529 | #2, #8, #9 | - | 144 | 2013.02 |
| 7 | 古交 | GJ02 | 2023.02 | 489 | #2, #8, #9 | - | 168 | 2013.02 |
| 8 | 古交 | GJ01 | 2023.02 | 452 | #2, #8 | - | 336 | 2013.02 |
| 9 | 古交 | GJ11 | 2023.02 | 521 | #8, #9 | - | - | - |
| 10 | 古交 | XSFH* | 2023.02 | - | - | - | - | - |
| 11 | 阳泉 | YQ01 | 2023.02 | 385 | - | - | - | 2011.10 |
| 12 | 阳泉 | YQ04 | 2023.02 | 618 | #15 | - | 600 | 2009.10 |
| 13 | 阳泉 | YQ03 | 2023.02 | 653 | #8, #9, #15 | - | 240 | 2009.04 |
| 14 | 阳泉 | YQ02 | 2023.02 | 713 | #8, #9, #15 | - | 240 | 2009.05 |
| 15 | 阳泉 | YQ11 | 2023.02 | 652 | #8, #15 | - | 240 | 2010.10 |
| 16 | 阳泉 | YQ12 | 2023.02 | 569 | #9, #15 | - | 240 | 2011.01 |
| 17 | 阳泉 | YQ05 | 2023.02 | 688 | #15 | - | 192 | 2010.04 |
| 18 | 阳泉 | YQ08 | 2023.02 | 663 | #8, #15 | - | 480 | 2010.11 |
| 19 | 榆社 | YS07 | 2023.02 | 1 579 | #2, #3, #9, #12, #15 | 1.43×106 | 2 006 | 2021.01 |
| 20 | 榆社 | YS08 | 2023.02 | 1 458 | #2, #3, #15 | 5.22×105 | 2 532 | 2021.08 |
| 21 | 榆社 | YS09 | 2023.02 | 1 491 | #9, #12, #15 | 7.51×105 | 3 030 | 2021.08 |
| 22 | 榆社 | 2302Y1 | 2023.02 | 1 545 | #3, #12, #15 | 6.08×104 | 493 | 2021.11 |
| 23 | 榆社 | 2207Y1 | 2022.07 | 1 545 | #3, #12, #15 | - | - | - |
| 24 | 榆社 | YS04 | 2023.02 | 1 518 | #3, #15 | 6.24×105 | 1 032 | 2021.05 |
| 25 | 榆社 | YS01 | 2023.02 | 1 251 | #2, #3, #15 | 5.01×105 | 370 | 2020.12 |
| 26 | 榆社 | YS02 | 2023.02 | 1 253 | #3, #15 | 3.00×105 | 274 | 2020.12 |
| 27 | 榆社 | 2207Y2 | 2022.07 | 1 514 | #15 | - | - | - |
| 28 | 榆社 | 2302Y2 | 2023.02 | 1 514 | #15 | 6.54×104 | 514 | 2021.12 |
| 29 | 柿庄 | SZ01 | 2022.07 | 716 | #3 | 1.90×106 | - | 2010.07 |
| 30 | 柿庄 | SZ12 | 2022.07 | 824 | #3 | 1.00×106 | - | 2012.11 |
| 31 | 柿庄 | SZ11 | 2022.07 | 772 | #3 | 9.70×105 | - | 2012.11 |
| 32 | 柿庄 | SZ09 | 2022.07 | 740 | #3 | 1.30×106 | - | 2012.09 |
| 33 | 柿庄 | SZ07 | 2022.07 | 709 | #3 | 1.30×106 | - | 2012.09 |
| 34 | 柿庄 | SZ07 | 2022.07 | 717 | #3 | 1.20×106 | - | 2012.09 |
| 35 | 郑庄 | ZZ10 | 2022.07 | 1 753 | #15 | 1.50×105 | - | 2012.12 |
| 36 | 郑庄 | ZZ11 | 2022.07 | 1 793 | #15 | 3.99×105 | - | 2021.12 |
| 37 | 郑庄 | ZZ15 | 2022.07 | 2 006 | #15 | 1.33×105 | - | 2020.11 |
| 38 | 郑庄 | ZZ14 | 2022.07 | 1 946 | #15 | 3.30×105 | - | 2020.11 |
| 39 | 郑庄 | ZZ13 | 2022.07 | 1 738 | #3 | 3.76×106 | - | 2020.11 |
| 40 | 郑庄 | HHHS* | 2022.07 | - | - | - | - | - |
| 41 | 郑庄 | ZZ01 | 2022.07 | 1 956 | #15 | 2.12×106 | - | 2019.11 |
| 42 | 郑庄 | ZZ04 | 2022.07 | 1 668 | #3 | 2.90×106 | - | 2021.05 |
| 43 | 郑庄 | ZZ05 | 2022.07 | 1 872 | #15 | 3.08×106 | - | 2021.05 |
| 44 | 郑庄 | ZZ03 | 2022.07 | 1 813 | #15 | 1.33×106 | - | 2021.10 |
| 45 | 郑庄 | ZZ08 | 2022.07 | 1 564 | #15 | 2.63×105 | - | 2021.03 |
| 46 | 郑庄 | ZZ07 | 2022.07 | 1 630 | #3 | 9.99×105 | - | 2021.03 |
| 47 | 郑庄 | ZZ12 | 2022.07 | 1 658 | #15 | 3.17×105 | - | 2022.03 |
| 48 | 郑庄 | ZZ06 | 2022.07 | 1 657 | #3 | 2.04×105 | - | 2022.03 |
| 49 | 潘庄 | PZ01 | 2022.07 | 568 | #3, #9, #15 | 2.28×106 | - | 2009 |
| 50 | 潘庄 | PZ02 | 2022.07 | 560 | #9, #15 | 1.31×105 | - | 2019 |
| 51 | 潘庄 | PZ03 | 2022.07 | 521 | #3, #9, #15 | 1.14×106 | - | 2009 |
| 52 | 潘庄 | PZ04 | 2022.07 | 398 | #3, #9, #15 | 5.78×106 | - | 2010 |
| 53 | 潘庄 | PZ06 | 2022.07 | 524 | #9, #15 | 1.05×106 | - | 2018 |
| 54 | 潘庄 | PZ05 | 2022.07 | 421 | #15 | 2.28×106 | - | 2020 |
| 55 | 潘庄 | PZ07 | 2022.07 | 468 | #9, #15 | 2.31×106 | - | 2017.09 |
| 56 | 潘庄 | PZ08 | 2022.07 | 516 | #9, #15 | 3.13×106 | - | 2017.09 |
| 57 | 潘庄 | PZ09 | 2022.07 | 503 | #9, #15 | 8.42×105 | - | 2017.09 |
| 58 | 潘庄 | PZ10 | 2022.07 | 1 133 | #15 | 5.70×106 | - | 2019.12 |
| 59 | 潘庄 | PZ11 | 2022.07 | 442 | #15 | 1.40×107 | - | 2015.02 |
| 60 | 潘庄 | QHPZ* | 2022.07 | - | - | - | - | - |
|
表2 沁水盆地煤层气井排采水的化学组成及矿物饱和系数Table 2 Chemical compositions and selected mineral saturation index of CBM co-produced water from Qinshui Basin |
| 样品 编号 | EC/(μs/cm) | 温度 /ºC | pH | Na+/ (mmol/L) | K+ / (mmol/L) | Mg2+ / (mmol/L) | Ca2+ / (mmol/L) | Cl-/ (mmol/L) | SO4 2-/ (mmol/L) | NO3 -/ (mmol/L) | CO3 2-/ (mmol/L) | HCO3 -/(mmol/L) | SI(Halite) | SI(Calcite) | SI(Dolomite) | SI(Gypsum) |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| GJ08 | 1 403 | 11 | 8.55 | 14.50 | 0.04 | 0.02 | 0.01 | 3.40 | 0.06 | - | 0.22 | 10.28 | -5.97 | -0.82 | -1.46 | -5.14 |
| GJ06 | 1 032 | 13.4 | 8.71 | 10.77 | 0.02 | 0.01 | 0.01 | 2.82 | 0.01 | 0.00 | 0.21 | 7.10 | -6.17 | -0.76 | -1.76 | -5.73 |
| GJ07 | 1 239 | 11.8 | 8.53 | 12.97 | 0.02 | 0.02 | 0.01 | 2.82 | 0.08 | 0.01 | 0.19 | 9.47 | -6.1 | -0.85 | -1.48 | -4.95 |
| GJ05 | 1 409 | 5.2 | 8.77 | 15.00 | 0.04 | 0.03 | 0.03 | 3.62 | 0.03 | 0.01 | 0.36 | 10.32 | -5.92 | -0.19 | -0.61 | -4.97 |
| GJ04 | 1 568 | 14.8 | 8.35 | 16.95 | 0.04 | 0.03 | 0.02 | 2.91 | 0.03 | 0.01 | 0.18 | 13.41 | -5.98 | -0.69 | -1.12 | -5.34 |
| GJ03 | 1 310 | 6.1 | 8.90 | 13.40 | 0.02 | 0.03 | 0.03 | 3.89 | 0.03 | 0.01 | 0.38 | 8.32 | -5.94 | -0.12 | -0.43 | -4.92 |
| GJ02 | 1 495 | 10.5 | 7.91 | 15.52 | 0.03 | 0.04 | 0.06 | 4.29 | 0.03 | 0.01 | 0.05 | 10.86 | -5.84 | -0.65 | -1.55 | -4.7 |
| GJ01 | 1 590 | 16.5 | 8.69 | 16.65 | 0.03 | 0.03 | 0.03 | 3.36 | 0.03 | 0.01 | 0.35 | 11.97 | -5.93 | -0.15 | -0.2 | -5.11 |
| GJ11 | 5 940 | 12.7 | 8.06 | 57.60 | 0.90 | 0.21 | 0.34 | 36.46 | 0.05 | 0.02 | 0.40 | 22.44 | -4.42 | 0.42 | 0.59 | -3.97 |
| XSFH* | 780 | 2.4 | 8.33 | 1.33 | 0.04 | 0.75 | 2.66 | 0.71 | 1.67 | 0.18 | 0.05 | 4.54 | -7.67 | 0.91 | 1.02 | -1.23 |
| YQ01 | 1 361 | 12.0 | 9.09 | 15.18 | 0.03 | 0.02 | 0.03 | 1.50 | 0.03 | 0.01 | 0.87 | 11.62 | -6.31 | 0.09 | 0.11 | -5.16 |
| YQ04 | 1 654 | 10.3 | 8.77 | 18.95 | 0.05 | 0.04 | 0.08 | 1.03 | 0.03 | 0.01 | 0.62 | 16.91 | -6.39 | 0.43 | 0.44 | -4.66 |
| YQ03 | 1 849 | 14.5 | 8.91 | 20.82 | 0.03 | 0.03 | 0.05 | 1.11 | 0.03 | 0.01 | 0.87 | 17.08 | -6.32 | 0.37 | 0.51 | -4.92 |
| YQ02 | 1 569 | 14.4 | 8.70 | 18.12 | 0.03 | 0.03 | 0.05 | 1.09 | 0.04 | 0.01 | 0.48 | 15.60 | -6.38 | 0.18 | 0.13 | -4.73 |
| YQ11 | 1 554 | 13.7 | 8.66 | 17.93 | 0.02 | 0.03 | 0.03 | 1.20 | 0.03 | 0.01 | 0.44 | 15.59 | -6.34 | -0.04 | -0.16 | -5.06 |
| YQ12 | 1 504 | 11.6 | 8.77 | 17.30 | 0.02 | 0.03 | 0.03 | 1.12 | 0.03 | 0.01 | 0.54 | 14.73 | -6.39 | -0.02 | -0.14 | -5.06 |
| YQ05 | 1 685 | 17.3 | 8.86 | 19.36 | 0.02 | 0.02 | 0.03 | 1.19 | 0.03 | 0.01 | 0.75 | 16.49 | -6.32 | 0.14 | 0.25 | -5.16 |
| YQ08 | 1 934 | 11.5 | 8.74 | 20.82 | 0.02 | 0.03 | 0.06 | 5.22 | 0.03 | 0.01 | 0.48 | 14.32 | -5.64 | 0.2 | 0.1 | -4.7 |
| YS07 | 9 090 | 6.8 | 7.93 | 88.46 | 1.80 | 0.15 | 0.05 | 67.62 | 0.22 | 0.04 | 0.13 | 23.94 | -3.99 | -0.65 | -0.98 | -4.24 |
| YS08 | 6 700 | 7.4 | 7.70 | 61.94 | 1.52 | 0.07 | 0.01 | 46.40 | 0.15 | 0.04 | 0.10 | 13.97 | -4.28 | -1.74 | -2.74 | -4.99 |
| YS09 | 19 830 | 6.7 | 8.08 | 189.16 | 2.52 | 0.99 | 0.73 | 183.56 | 0.55 | - | 0.06 | 18.85 | -3.27 | 0.42 | 0.84 | -2.93 |
| 2302Y1 | 3 480 | 35.6 | 8.14 | 36.39 | 0.28 | 0.03 | 0.01 | 13.79 | 0.05 | 0.02 | 0.21 | 23.08 | -5.04 | -0.71 | -0.75 | -5.44 |
| 2207Y1 | 4 170 | 19.4 | 8.18 | 42.98 | 0.44 | 0.04 | 0.17 | 21.61 | 0.16 | - | 1.08 | 23.19 | -4.76 | 0.36 | 0.17 | -3.75 |
| YS04 | 17 100 | 22.4 | 7.93 | 166.63 | 1.58 | 0.55 | 0.43 | 158.54 | 0.52 | - | 0.07 | 14.29 | -3.4 | 0.18 | 0.58 | -3.18 |
| YS01 | 3 810 | 11.9 | 8.48 | 37.19 | 0.84 | 0.03 | 0.01 | 19.66 | 0.06 | 0.02 | 0.35 | 18.30 | -4.85 | -0.76 | -1.12 | -5.3 |
| YS02 | 2 660 | 11.8 | 8.42 | 26.54 | 0.52 | 0.03 | 0.01 | 8.10 | 0.06 | 0.02 | 0.33 | 19.30 | -5.36 | -0.76 | -1.11 | -5.24 |
| 2207Y2 | 4 110 | 16.0 | 7.71 | 43.76 | 0.10 | 0.09 | 0.40 | 16.23 | 0.23 | - | 0.00 | 29.34 | -4.88 | 0.32 | 0.02 | -3.2 |
| 2302Y2 | 4 000 | 13 | 8.04 | 42.97 | 0.08 | 0.04 | 0.01 | 15.90 | 0.05 | 0.02 | 0.20 | 27.47 | -4.89 | -1.02 | -1.49 | -5.41 |
| SZ01 | 1 575 | 25.2 | 7.89 | 15.83 | 0.05 | 0.07 | 0.23 | 6.13 | 0.04 | - | 0.32 | 10.28 | -5.7 | 0.11 | -0.16 | -3.93 |
| SZ12 | 1 743 | 21.8 | 8.67 | 19.47 | 0.15 | 0.02 | 0.10 | 2.51 | 0.04 | - | 1.85 | 15.98 | -6 | 0.57 | 0.48 | -4.44 |
| SZ11 | 5 410 | 21.1 | 8.67 | 66.91 | 0.07 | 0.07 | 0.28 | 3.85 | 0.06 | 0.05 | 9.56 | 58.63 | -5.36 | 1.24 | 2.01 | -4.3 |
| SZ09 | 1 225 | 21.5 | 8.30 | 13.06 | 0.02 | 0.03 | 0.10 | 2.22 | 0.03 | 0.03 | 0.36 | 10.82 | -6.21 | 0.12 | -0.19 | -4.5 |
| SZ07 | 2 090 | 35.5 | 8.43 | 23.25 | 0.04 | 0.02 | 0.06 | 4.58 | 0.04 | - | 1.53 | 17.81 | -5.69 | 0.3 | 0.29 | -4.74 |
| SZ07 | 1 649 | 28.6 | 8.79 | 18.01 | 0.07 | 0.02 | 0.08 | 3.92 | 0.24 | - | 2.05 | 12.65 | -5.85 | 0.57 | 0.74 | -3.77 |
| ZZ10 | 3 850 | 22.3 | 7.79 | 36.88 | 0.43 | 0.82 | 1.05 | 17.68 | 0.88 | - | 1.42 | 23.27 | -4.92 | 0.83 | 1.66 | -2.23 |
| ZZ11 | 5 350 | 21.3 | 7.81 | 49.84 | 1.65 | 1.05 | 1.22 | 32.82 | 0.22 | - | 1.58 | 25.17 | -4.54 | 0.9 | 1.83 | -2.83 |
| ZZ15 | 4 430 | 22.0 | 8.03 | 43.17 | 1.14 | 0.53 | 0.74 | 23.59 | 0.00 | 0.05 | 1.38 | 24.77 | -4.73 | 0.92 | 1.8 | - |
| ZZ14 | 4 110 | 21.5 | 7.88 | 41.91 | 0.26 | 0.33 | 0.47 | 19.46 | 0.16 | 0.05 | 0.00 | 25.64 | -4.82 | 0.58 | 1.1 | -3.29 |
| ZZ13 | 5 280 | 23.2 | 8.02 | 53.88 | 0.12 | 0.19 | 0.30 | 34.17 | 0.24 | - | 0.00 | 23.10 | -4.49 | 0.47 | 0.86 | -3.38 |
| HHHS* | 628 | 18.8 | 8.27 | 0.74 | 0.04 | 0.74 | 2.16 | 0.59 | 1.07 | 0.35 | 0.36 | 3.63 | -8.01 | 0.97 | 1.52 | -1.53 |
| ZZ01 | 3 270 | 26.8 | 7.50 | 34.51 | 0.36 | 0.24 | 0.28 | 10.82 | 0.47 | 0.05 | 0.00 | 25.07 | -5.16 | 0.07 | 0.22 | -3.02 |
| ZZ04 | 8 910 | 29.7 | 8.65 | 82.02 | 4.95 | 0.29 | 0.55 | 78.97 | 0.52 | - | 3.20 | 13.27 | -3.98 | 1.14 | 2.22 | -2.96 |
| ZZ05 | 8 520 | 22.5 | 7.79 | 66.44 | 11.05 | 0.77 | 1.25 | 67.99 | 0.54 | 0.14 | 0.00 | 20.83 | -4.12 | 0.76 | 1.42 | -2.52 |
| ZZ03 | 3 640 | 23.4 | 7.87 | 37.04 | 0.58 | 0.39 | 0.42 | 16.25 | 0.00 | 0.05 | 0.79 | 23.08 | -4.95 | 0.54 | 1.16 | - |
| ZZ08 | 2 810 | 21.4 | 7.86 | 27.50 | 1.68 | 0.53 | 0.54 | 7.13 | 0.25 | - | 0.00 | 24.16 | -5.42 | 0.63 | 1.35 | -2.99 |
| ZZ07 | 5 030 | 20.1 | 8.26 | 52.47 | 1.92 | 0.27 | 0.29 | 23.09 | 0.00 | - | 1.46 | 33.01 | -4.67 | 0.78 | 1.61 | - |
| ZZ12 | 4 940 | 22.1 | 7.37 | 47.06 | 0.30 | 0.45 | 0.74 | 31.82 | 0.22 | - | 0.00 | 20.21 | -4.57 | 0.18 | 0.25 | -2.99 |
| ZZ06 | 4 130 | 20.1 | 7.44 | 41.79 | 0.11 | 0.17 | 0.26 | 23.53 | 0.18 | - | 0.00 | 20.71 | -4.74 | -0.19 | -0.51 | -3.47 |
| PZ01 | 2 200 | 20.3 | 7.98 | 17.32 | 0.08 | 1.75 | 0.63 | 1.77 | 6.33 | 0.03 | 0.43 | 11.38 | -6.23 | 0.44 | 1.39 | -1.55 |
| PZ02 | 2 030 | 20.4 | 8.55 | 18.57 | 0.66 | 0.59 | 0.58 | 3.46 | 4.37 | 0.03 | 1.16 | 9.45 | -5.9 | 0.93 | 1.94 | -1.71 |
| PZ03 | 2 190 | 23.7 | 8.96 | 19.19 | 1.99 | 0.27 | 0.22 | 7.02 | 2.83 | - | 1.93 | 9.52 | -5.58 | 0.92 | 2.07 | -2.36 |
| PZ04 | 1 304 | 21.8 | 8.90 | 14.28 | 0.02 | 0.04 | 0.02 | 1.93 | 0.05 | 0.03 | 1.63 | 11.49 | -6.24 | 0.05 | 0.43 | -4.9 |
| PZ06 | 2 410 | 20.0 | 7.54 | 2.59 | 0.08 | 5.27 | 9.17 | 0.42 | 15.10 | 0.03 | 0.00 | 2.81 | -7.7 | 0.45 | 0.71 | -0.21 |
| PZ05 | 1 403 | 19.1 | 8.79 | 14.79 | 0.10 | 0.22 | 0.22 | 1.61 | 0.16 | - | 2.19 | 13.03 | -6.3 | 0.92 | 1.93 | -3.47 |
| PZ07 | 1 945 | 26.0 | 8.58 | 20.37 | 0.10 | 0.31 | 0.24 | 4.80 | 0.07 | - | 2.06 | 15.37 | -5.71 | 0.89 | 2.07 | -3.83 |
| PZ08 | 2 310 | 21.8 | 8.77 | 25.13 | 0.08 | 0.11 | 0.09 | 6.22 | 0.84 | - | 2.40 | 16.53 | -5.52 | 0.55 | 1.33 | -3.28 |
| PZ09 | 1 853 | 29.5 | 8.68 | 20.98 | 0.03 | 0.06 | 0.04 | 1.42 | 0.06 | 0.03 | 2.23 | 17.98 | -6.23 | 0.21 | 0.89 | -4.84 |
| PZ10 | 2 080 | 18.3 | 8.66 | 22.48 | 0.32 | 0.09 | 0.06 | 3.91 | 1.36 | - | 2.06 | 15.84 | -5.76 | 0.28 | 0.77 | -3.15 |
| PZ11 | 1 956 | 19.1 | 8.67 | 21.17 | 0.19 | 0.08 | 0.05 | 3.91 | 1.16 | 0.03 | 1.76 | 14.49 | -5.78 | 0.19 | 0.63 | -3.29 |
| QHPZ* | 503 | 34.2 | 8.51 | 1.14 | 0.06 | 0.69 | 1.40 | 0.85 | 1.02 | 0.29 | 0.00 | 2.55 | -7.67 | 1.03 | 1.96 | -1.72 |
|
表3 沁水盆地煤层气井排采水的同位素组成Table 3 Isotopic compositions of CBM co-produced water from Qinshui Basin |
| 样品编号 | /‰ | /‰ | δ13CDIC/‰ | Δ14CDIC/‰ |
|---|---|---|---|---|
| GJ08 | -10.82 | -82.21 | 27.14 | -995.8 |
| GJ06 | -10.79 | -83.31 | 7.65 | -989.1 |
| GJ07 | -10.40 | -77.93 | 22.06 | -954.4 |
| GJ05 | -11.66 | -85.90 | 27.05 | -994.4 |
| GJ04 | -11.05 | -80.96 | 30.69 | -992.1 |
| GJ03 | -12.04 | -86.83 | 19.43 | -988.6 |
| GJ02 | -11.62 | -84.38 | 30.59 | -982.7 |
| GJ01 | -11.52 | -82.88 | 29.47 | -984.5 |
| GJ11 | -10.75 | -73.75 | 30.05 | -991.9 |
| XSFH* | -9.36 | -66.48 | -10.89 | -75.3 |
| YQ01 | -11.00 | -80.52 | 22.64 | - |
| YQ04 | -10.25 | -68.13 | 21.00 | - |
| YQ03 | -10.71 | -72.33 | 20.84 | - |
| YQ02 | -10.73 | -72.09 | 19.75 | - |
| YQ11 | -10.87 | -73.95 | 19.39 | - |
| YQ12 | -11.01 | -78.26 | 22.93 | - |
| YQ05 | -10.75 | -72.46 | 20.58 | - |
| YQ08 | -10.73 | -71.03 | 20.41 | - |
| YS07 | -9.60 | -66.43 | 12.62 | -997.5 |
| YS08 | -7.97 | -57.03 | 34.80 | -985.0 |
| YS09 | -9.61 | -67.82 | 32.90 | -995.9 |
| 2302Y1 | -9.68 | -67.54 | 32.36 | -989.4 |
| 2207Y1 | -7.50 | -54.39 | 7.12 | -994.2 |
| YS04 | -10.73 | -76.04 | 19.96 | -993.5 |
| YS01 | -10.83 | -77.16 | 19.64 | -996.9 |
| YS02 | -9.28 | -64.73 | 29.07 | -989.2 |
| 2207Y2 | -9.61 | -67.53 | 29.17 | - |
| 2302Y2 | -9.40 | -65.88 | 27.72 | - |
| SZ01 | -11.26 | -81.47 | 12.32 | - |
| SZ12 | -11.18 | -80.35 | 31.66 | - |
| SZ11 | -11.22 | -80.33 | -4.19 | - |
| SZ09 | -11.30 | -81.50 | 11.57 | - |
| SZ07 | -10.76 | -77.54 | 24.65 | - |
| SZ07 | -11.00 | -79.25 | 30.63 | - |
| ZZ10 | -10.85 | -74.25 | -1.99 | - |
| ZZ11 | -10.15 | -70.16 | -0.80 | - |
| ZZ15 | -10.46 | -71.33 | -0.20 | - |
| ZZ14 | -10.14 | -69.65 | 1.24 | - |
| ZZ13 | -9.86 | -66.36 | 21.61 | - |
| HHHS* | -8.98 | -64.47 | -9.71 | - |
| ZZ01 | -10.19 | -68.05 | 2.80 | - |
| ZZ04 | -8.53 | -57.07 | 14.22 | - |
| ZZ05 | -9.79 | -66.17 | 6.83 | - |
| ZZ03 | -10.41 | -69.58 | 0.84 | - |
| ZZ08 | -10.67 | -71.98 | 8.30 | - |
| ZZ07 | -10.06 | -66.99 | 22.23 | - |
| ZZ12 | -10.34 | -70.32 | 2.43 | - |
| ZZ06 | -10.48 | -70.52 | 16.44 | - |
| PZ01 | -10.95 | -79.68 | 5.91 | - |
| PZ02 | -10.53 | -77.36 | 7.32 | - |
| PZ03 | -10.30 | -75.59 | 5.76 | - |
| PZ04 | -10.71 | -78.78 | 9.71 | - |
| PZ06 | -9.71 | -71.00 | -2.63 | - |
| PZ05 | -10.98 | -80.28 | 4.45 | - |
| PZ07 | -10.54 | -76.39 | 13.52 | - |
| PZ08 | -10.53 | -74.67 | 13.90 | - |
| PZ09 | -10.49 | -74.53 | 15.39 | - |
| PZ10 | -10.84 | -78.38 | 14.46 | - |
| PZ11 | -10.53 | -75.76 | 15.60 | - |
| QHPZ* | -8.20 | -59.18 | -8.73 | - |
|
4 讨论
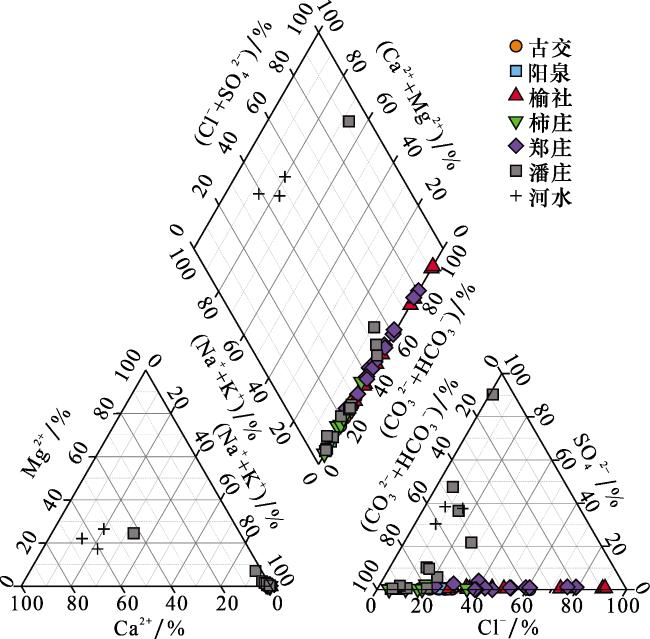
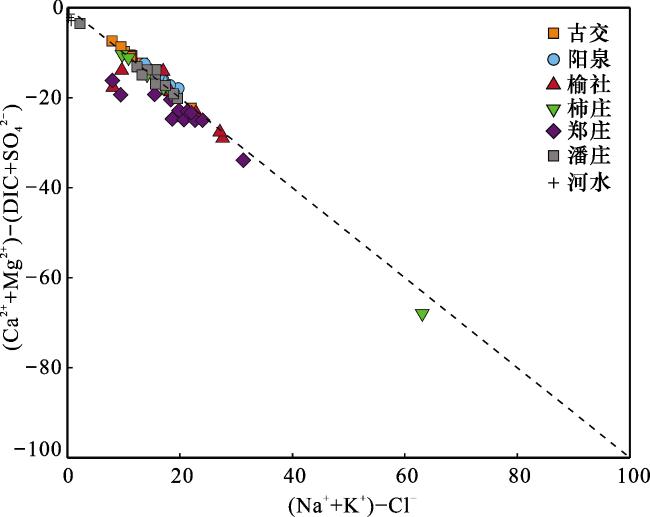
4.1 沁水盆地煤层气井排采水的来源
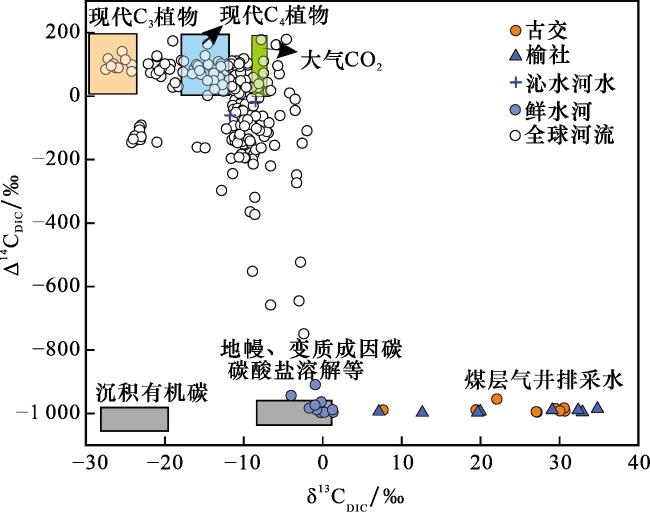
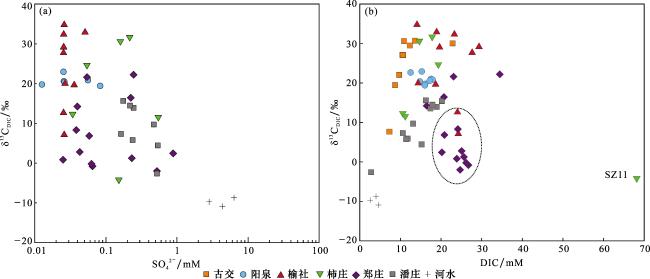
4.2 沁水盆地煤层气井排采水中无机溶解碳的来源
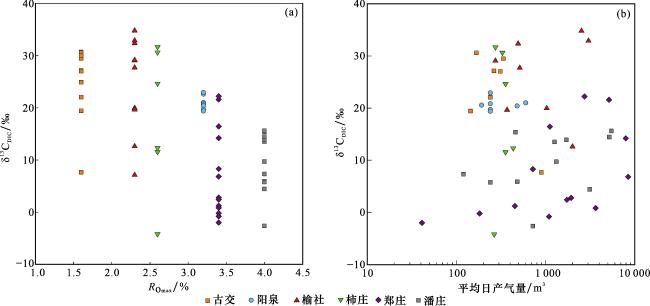
4.3 沁水盆地次生生物甲烷的地球化学约束
表4 溶解无机碳同位素组成和镜质体反射率数据统计结果Table 4 Summary of δ13CDIC and R Omax from worldwide CBM co-produced water |
| 样品位置 | R O/% | δ13CDIC /‰ | 数据来源 |
|---|---|---|---|
| 沁水盆地 | 0.5~4 | -4.2~34.8 | 本研究 |
| 沁水(柿庄南) | 2.5 | -11.9~24.5 | 文献[45] |
| 沁水(柿庄) | - | 20.0 (max.) | 文献[17] |
| 黔西 | 1.4~3.6 | -6.7~27.2 | 文献[58] |
| 阜新盆地 | 0.4~0.6 | -0.1~1.6 | 文献[52] |
| Powder River Basin | - | -12.7~24.1 | 文献[60] |
| - | - | 12~22 | 文献[48] |
| Forest City Basin | 0.5~0.7 | 2.8~13.1 | 文献[9] |
| Atlantic Rim | - | -3.6~22.8 | 文献[54] |
| Alberta Basin | 0.4~0.75 | 20.0 (av.) | 文献[55] |
| Illinois Basin | 0.5~0.9 | -13.5~35.1 | 文献[56] |
| Surat Basin | 0.35~0.7 | -10.8~25.9 | 文献[61] |
| Cesar Rancheria Basin | 0.39~0.53 | -0.9~9.7 | 文献[57] |
|


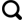
 甘公网安备 62010202000678号
甘公网安备 62010202000678号